慢性疼痛涉及躯体感觉和情感方面的不愉快经历,伴随着前额叶皮层(PFC)神经可塑性改变。然而,特异性PFC神经元集合是否是慢性疼痛的基础仍然未知。
2022年12月,北京大学伊鸣老师和万有老师团队合作于国际著名期刊Cell Reports发表了题为“A nociceptive neuronal ensemble in the dorsomedial prefrontal cortex underlies pain chronicity”的研究论文。在本研究中,作者发现背侧前额叶皮层(dmPFC)存在一群对伤害性刺激具有显著反应的神经元集群,利用微型化双光子技术记录了自由行为小鼠慢性炎症疼痛前后dmPFC脑区单个神经元水平的实时反应。并通过进一步研究发现,这个特异性神经元群体拥有独特的分子特征,与疼痛相关区域包括基底外侧杏仁核(BLA)和臂旁外侧核(LPB)密集相连。这群神经元的长时间化学遗传激活可在正常小鼠中诱导慢性疼痛样行为,沉默这群细胞则可以缓解患有慢性炎症性疼痛小鼠的疼痛超敏反应和焦虑。

作者利用cfos-htTA小鼠,发现当伤害性激光刺激诱导小鼠的伤害性反应后,dmPFC中部分神经元出现了显著的激活,此前研究中发现的BLA等被激活侧面说明了这一结果的真实性。
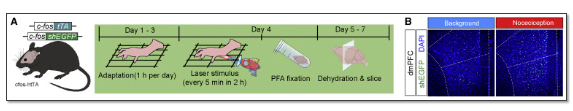
图1 实验方案:使用cfos-htTA转基因小鼠进行后爪激光刺激诱导并进行神经元活动筛选
为了探究dmPFC在急性和慢性疼痛中的编码机制,作者利用微型化双光子显微成像系统(FHIRM-TPM V2.0)观测慢性痛造模前后单个神经元对疼痛刺激的实时反应。借助于基因编码探针GCaMP6s和Grin Lens植入技术,实现了对dmPFC脑区神经元钙信号的长期稳定观测。
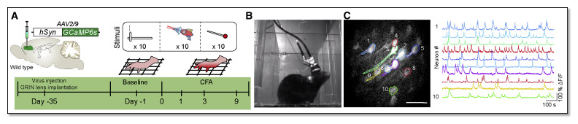
图2 (A-C)CFA诱导炎症性疼痛中dmPFC神经元活性的双光子成像实验方案
研究发现,在基线条件下足部刺激(Von Frey)和激光刺激均可显著诱导dmPFC中12.9%和12.8%的神经元活动,将这类对伤害性刺激有反应的细胞群体视为dmPFC伤害性神经元集合。而在足底注射弗氏佐剂后,更多的dmPFC神经元对伤害性刺激产生了显著的反应;在CFA注射后的第1天,分别有21.3%和19.1%的dmPFC神经元对足部刺激和激光反应有响应。激活的dmPFC神经元的比例在炎症性疼痛的后期(第3-9天)逐渐降低,同时从异常性疼痛中恢复。触觉刺激也观察到类似的趋势。重要的是,对dmPFC神经元集合的长期跟踪显示,在注射CFA后激活的神经元群体一直在后续的多天足部刺激中具有明显的响应,这表明该上伤害性神经元集合可能参与了慢性疼痛的编码。

图3 炎症性疼痛模型中微型化双光子成像记录dmPFC的各神经元钙离子活动数据(D)及响应不同刺激的神经元集群分析(E-K)
为了进一步研究这一群特异性神经元的特点,作者对dmPFC伤害性神经元进行了遗传标记,发现与背景标记神经元(包括Oprl1,Htr1f和几种嗅觉受体)相比,该dmPFC伤害性集合高度表达特定基因及部分嗅觉受体。基于dmPFC神经元顺行追踪结果及前人研究,作者选择了AcbC,BLA,PAG和LPB进行逆行追踪,发现这些脑区到dmPFC伤害感受集合的投射。作者利用化学遗传学长期人工激活dmPFC的伤害性神经元集合,在小鼠中引起了慢性疼痛样行为,包括机械异常性疼痛、热痛觉过敏以及焦虑。而在早期长期抑制这种dmPFC伤害性集合可以缓解炎症性疼痛中知觉超敏反应和焦虑的发展。
这项研究利用了多种实验手段和技术,发现dmPFC中的伤害性神经元集合在疼痛慢性中起着重要作用,并表明解剖不同神经元亚群在阐明每个大脑区域如何调节疼痛方面具有重要意义。
参考文献
Qi, X., Cui, K., Zhang, Y., Wang, L., Tong, J., Sun, W., Shao, S., Wang, J., Wang, C., Sun, X., et al. (2022). A nociceptive neuronal ensemble in the dorsomedial prefrontal cortex underlies pain chronicity. Cell Rep 41, 111833. 10.1016/j.celrep.2022.111833.



