定义
超声造影剂(Ultrasound Contrast Agents)是一类能够显著增强超声检测信号的诊断用药。临床中使用的超声造影剂是直径在微米量级的包膜微气泡。微泡与组织有很大的超声波回声差别,因此,经静脉注射微泡后可以得到增强血管对比度的超声图。超声造影可用于成像器官血流灌注、测量心脏及其他器官血流速度等。
微泡表面可以修饰靶向血管内特征性受体的配体,从而使微泡特异性地富集在靶向区域(例如患病或异常组织)中,这种超声分子成像技术也称为目标对比增强超声[1]。
在较高的超声强度下,微泡剧烈振荡,最终导致微泡的惯性空化。这种选择性的微泡靶向破坏技术(ultrasound-targeted microbubble destruction ,UTMD)已经成为组织再灌注成像的重要工具,特别是在超声心动图中评估梗死面积。同时,细胞附近的微泡破坏会导致细胞膜中瞬时形成孔,从而使化合物暂时被动扩散到细胞中,从而增强药物在细胞内的摄取,并将微泡携带的药物释放在靶向器官或组织血管内。
超声造影成像原理
声波在不同声介质之间传播时,会在界面处发生很强的背向散射。红细胞与血浆间的声压反射系数为(Ra)为1.3%,而气体与血浆之间的Ra为99.95%。因此,与组织相比,以气体为核心的微泡会产生很强的背向散射信号,从而在B-mode中得到很强的超声信号,在图像上更清晰的显示血管位置和大小[2]。
此外,液体中的微泡在超声波作用下吸收并散射能量的同时,还以自身固有的频率做膨胀与收缩震动。声波在组织中传播时,遇到规则界面,声波会发生反射和折射,即线性传播;遇到非规则界面,可发生波形畸变,谐波成分增多,声衰减系数增大,即非线性传播。因此,与组织相比,微泡在超声作用下可以产生更丰富的谐波信号。通过抑制基波,增强谐波,可以得到信噪比大大提高的超声谐波成像图像。
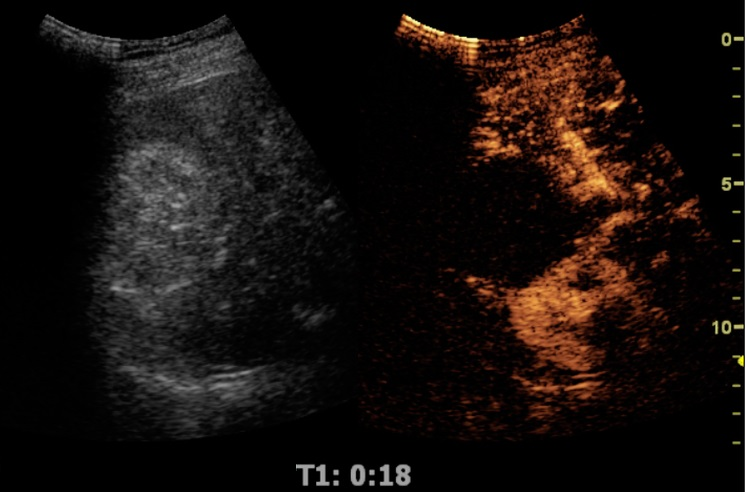
图 1 超声造影成像进行肾脏检查,在右图中未见肿瘤部位造影剂信号增强,表明成功用热消融治疗的肾细胞癌[1]。
超声造影剂的发展
超声造影剂的研究和应用可以追溯到1968年Gramiak[3]等人描述的心脏内注入盐水后可在主动脉根部得到云状回声对比效果。80年代后期,超声组织定征遇到一定的困难,某些组织即使病理上有区别,它们的超声特性却很相似。为此能增强组织和血液回波能力的超声造影剂受到极大关注。
早期的造影剂,包括含有自由气泡的液体;含有悬浮颗粒的胶状体;乳化液体等。缺点是尺寸大、不稳定、效果差。自由气泡是超声造影剂最简单的形式,中国临床采用过H2O2作为超声造影剂,它进入血液后生成游离氧,多用于心动学中的造影。由于自由气泡尺寸太大很不稳定,不能通过肺循环,不适于心脏造影。含悬浮颗粒的胶状体可用于增强软组织背向散射,且有较好的造影效果,它的存活时间长。但考虑到毒性的影响,只能小剂量使用,限制了其应用范围。脂类化合物作为超声造影剂是从脂肪肝的回波能力增强中得到的启示,它的增强效率较低。由许多化合物组成的水溶液进入人体后,使循环系统的声速和密度随造影剂的浓度发生变化,在脉管和非脉管组织间引起声阻抗差异,从而增强脉管系统的背向散射,但其增强效率太低。
90年代初以来,超声造影剂的研究工作取得了很大的进展。与早期的超声造影剂相比,直径为几个为你的可通过肺循环的包膜超声造影剂的应用效果最佳、应用范围更广、稳定性更好。而同时,世界上一些公司和研究机构研制了不同的超声造影剂,用于动物实验和临床研究的超声造影剂已投放市场。各种造影剂都能不同程度地增强组织的回波能力,并可用于谐波测量与成像。
造影剂的分代是主要是依据微泡内包裹气体的种类来划分的。第一代造影剂微泡内含空气,包膜一般为白蛋白或半乳糖等聚合体。第一代超声造影剂的物理特性,包括包膜较厚,弹性差,而且包裹的空气易溶于水等,决定了它持续时间短,容易破裂,从而限制了临床应用中观察和诊断的时间。第一代造影剂包括Albunex[4]、Echo-vist(SHU-454)和Levovist(SHU-508A)[5]。
目前第二代超声造影剂为包裹高密度惰性气体(不易溶于水或血液)为主的外膜薄而柔软的气泡,直径一般在2-5um左右,稳定时间长,振动及回波特性好。第二代造影剂包括Aerosomes(DMP-115)、EchoGen、Imagent(AFO150)、NC100100、Quantison、Sonovue(BR-1)[6-8]、AI-700、Bisphere、Sonovist(SHU-563A)、PESDA以及Optison(FS069)。

图 2 第一代超声造影剂结构图 |
图 3 第二代超声造影剂结构图 |
超声造影剂的种类
已被研究的超声造影剂主要有三大类[9]:

图 4 三种超声造影剂的空化机理示意图。
1、微泡
迄今为止,研究最广泛的超声造影剂是由表面活性剂、磷脂或聚合物涂层包裹的稳定气体微泡。微泡的直径一般为1-10μm,在室温(21℃)和常压(1atm)下,微泡的平均直径约为2μm,在生理温度(37℃)下,微泡会膨胀。
2、液滴
为了解决微泡在体积上的局限性,利用亚微米级的液滴形成微泡。液滴的液态核通常为低沸点全氟化碳,能够在超声波或激光激发下蒸发成为气态。常见的制备液地方式为冷凝法,即将制备好的微泡在4℃保存,使气核凝聚为液态,同时体积减小五倍左右。液滴的大小产生了一个高表面压力,使核保持在过热的液体状态。较小的体积使液滴能够在超声暴露前在血流中循环数十分钟,从而增加了治疗的窗口时间,与微泡相比靶向性更高。同时在与肿瘤相关的渗漏的脉管系统中液滴有更大的机会渗出,从而增大了其在组织中的渗透深度。
3、固体颗粒
另一种类型的超声造影剂是含有疏水空腔的固体颗粒,这些空腔可以捕获气体,从而提供成核位点。像液滴一样,这些颗粒的小尺寸有利于有利的增加循环时间和提高外渗的机率。已经研究的生物相容性固体颗粒有介孔硅[10]、碳纳米管[11]、polymer ‘sponges’ [12]、polymeric ’cups’ [13]和gold cones [14]。固体颗粒相对于气泡和液滴的一个主要优点是固体颗粒能够维持空化的程度,这是由于固体颗粒不会被超声波破坏。因此,只要疏水腔不被浸湿,粒子就可以连续地成泡。但由于疏水腔有被浸湿的风险及某些类型的颗粒存在安全隐患(如介孔二氧化硅可能诱发血栓形成、碳纳米管可能具有致癌性),固体颗粒作为超声造影剂仍是一个挑战。
超声造影剂必须具备的条件
1、无毒性,最终可降解或排出体外。
2、具有很强的散射特性。
3、其直径应足够小,小于红细胞的直径(7μm),确保能通过肺毛细血管,进入动脉循环,从而达到造影效果而不会造成栓塞。
4、具有足够的稳定性,在血液内保留的时间允许超声成像显示其在组织内的灌注(增强)和廓清(消退)过程。
5、有明确的破坏阈值,具有可预测性及可重复性,能够被较快地清除。
6、易于生产,便于储存,价格适宜。
参考文献
[1] https://zh.wikipedia.org/zh-hans/%E8%B6%85%E5%A3%B0%E9%80%A0%E5%BD%B1%E5%89%82
[2] Sboros V. Response of contrast agents to ultrasound[J]. Advanced drug delivery reviews, 2008, 60(10): 1117-1136.
[3] Gramiak R , Shah PM. Echocardiography of the aortic root[J].Invest Radiol, 1968 ,3(5):356-366.
[4] Krishna PD, Newhouse VL. Second harmonic characteristics of the ultrasound contrast agents albunex and FSO69. Ultrasound Med Biol 1997;23(3):453.
[5] Schlief R. Ultrasound contrast agents. Curr Opin Radiol 1991;3(2):198.
[6] Spinazzi A. Emerging clinical applications for contrast-enhanced ultrasonography. Eur Radiol 2001;11(Suppl. 3):E7.
[7] Correas JM, Bridal L, Lesavre A, Mejean A, Claudon M, Helenon O.Ultrasound contrast agents: properties, principles of action, tolerance, and artifacts. Eur Radiol 2001;11(8):1316.
[8] Schutt E, Klein D, Mattrey R, Riess J. Injectable microbubbles as contrast agents for diagnostic ultrasound imaging: the key role of perfluorochemicals. Angew Chem Int Ed Engl 2003;42:3218
[9] Stride E, Coussios C. Nucleation, mapping and control of cavitation for drug delivery[J]. Nature Reviews Physics, 2019, 1(8): 495-509.
[10] Paris, J. L. et al. Ultrasound-mediated cavitationenhanced extravasation of mesoporous silica nanoparticles for controlled-release drug delivery. Chem. Eng. J. 340, 2–8 (2018).
[11] Delogu, L. G. et al. Functionalized multiwalled carbon nanotubes as ultrasound contrast agents. Proc. Natl Acad. Sci. USA 109, 16612–16617 (2012).
[12] Straub, J. A. et al. Porous PLGA microparticles: AI-700, an intravenously administered ultrasound contrast agent for use in echocardiography. J. Control. Release 108, 21–32 (2005).
[13] Kwan, J. et al. Ultrasound-induced inertial cavitation from gas-stabilizing nanoparticles. Phys. Rev. E 92, 023019 (2015).
[14] Mannaris, C. et al. Gas-stabilizing gold nanocones for acoustically mediated drug delivery. Adv. Healthc. Mater. 7, 1800184 (2018).




